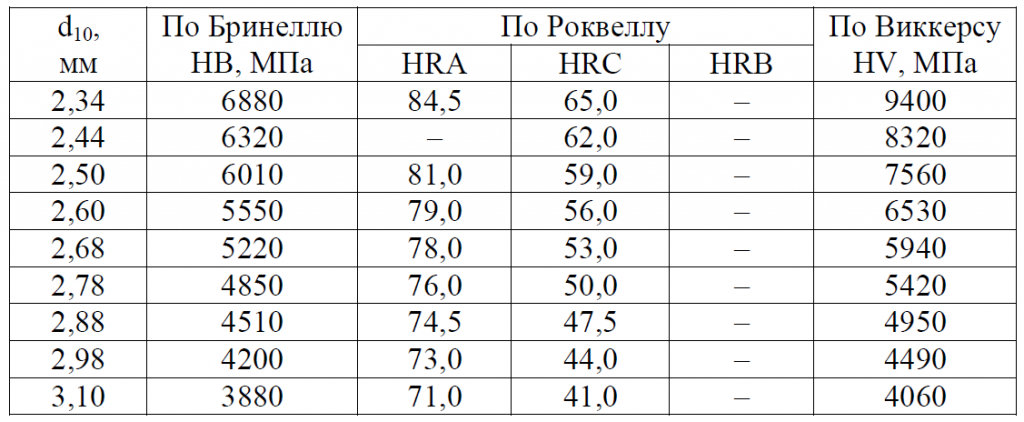
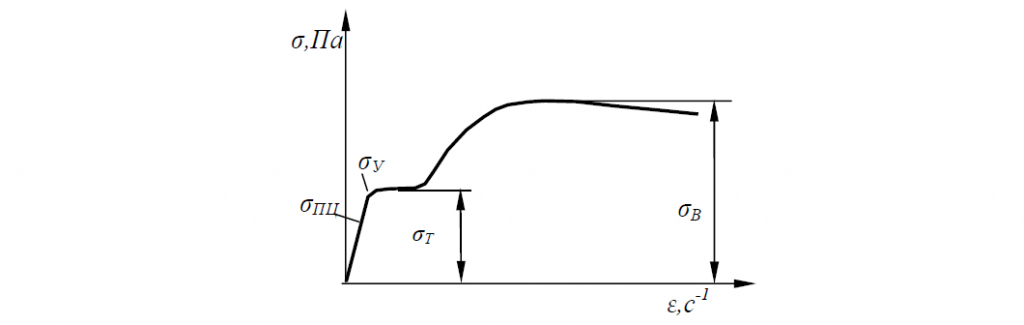
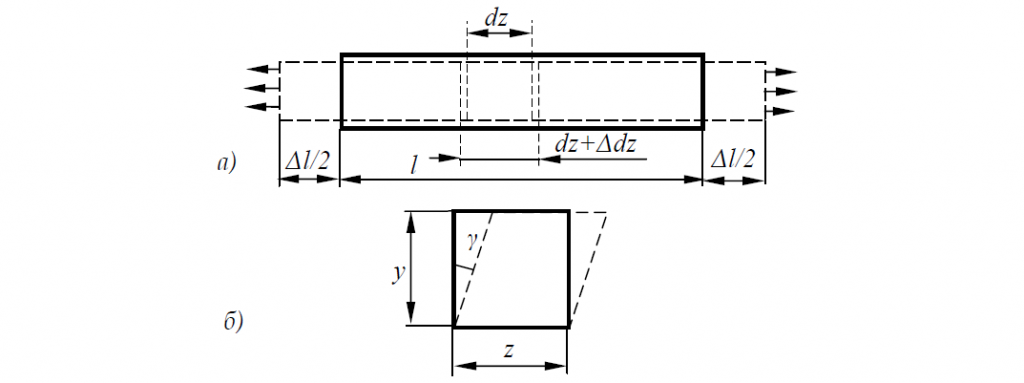
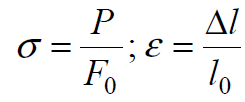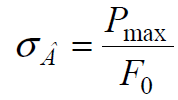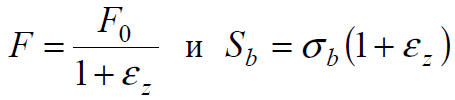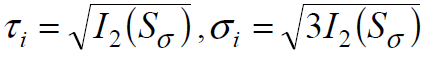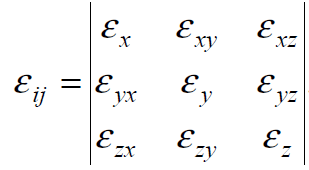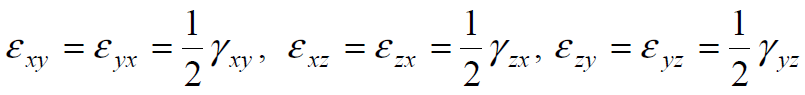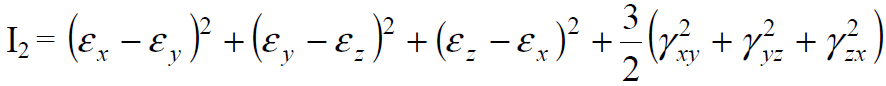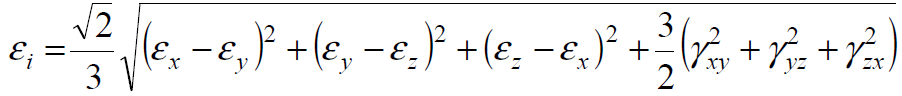Как следует из диаграмм растяжения, при деформации сталей при комнатной температуре предел текучести увеличивается с ростом деформации, то есть материал в этих условиях упрочняется.
Упрочнение — изменение структуры и свойств металлического материала. вызванное пластической деформацией.
Наибольшую сопротивляемость пластическому деформированию должен оказывать металл с очень малой плотностью дислокаций ρ. По мере увеличения плотности дислокаций ρ сопротивление пластическому деформированию уменьшается (рис. 1).
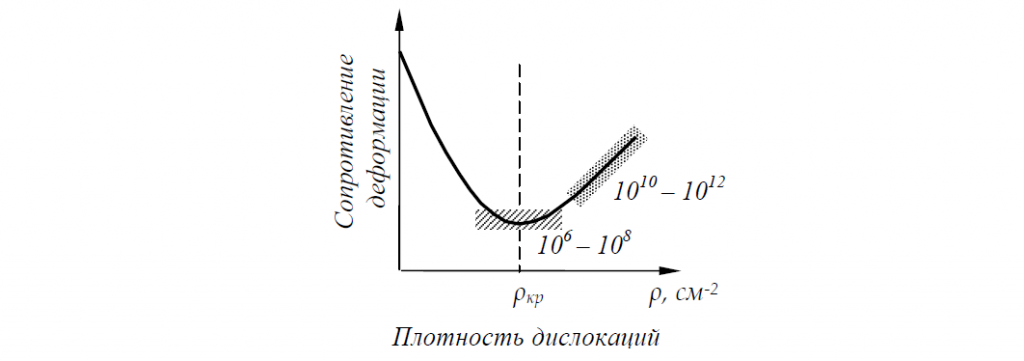
Это происходит до достижения некоторого критического значения плотности дислокаций ρкр, когда начинается взаимодействие силовых полей, окружающих дислокации, что и вызывает увеличение сопротивления пластическому деформированию.
Следовательно, увеличение сопротивления пластическому деформированию можно получить двумя путями: наклепом металла, т. е. прямым повышением плотности дислокаций или доведением плотности дислокаций до очень малого значения.
Наклепом называется упрочнение металла при холодной пластической деформации. В результате наклепа прочность (σв, σ0,2, твердость и др.) повышается, а пластичность и ударная вязкость (δ, ψ, KCU) — уменьшаются. Упрочнение возникает вследствие увеличения числа дефектов кристаллической структуры, которые затрудняют движение дислокаций, а следовательно, повышают сопротивление деформации и уменьшают пластичность.
Наклеп является одним из важнейших способов изменения свойств, особенно для сплавов, не упрочняющихся термической обработкой, и для металлов, обладающих пластичностью. Методы упрочняющего воздействия можно разделить на поверхностные (обкатка роликами, дробеструйная обработка) и сквозные (прокатка листов, волочение проволоки). Обработка металлов резанием также приводит к наклепу и изменению структуры в тонком поверхностном слое, что необходимо учитывать при последующей эксплуатации изделий.
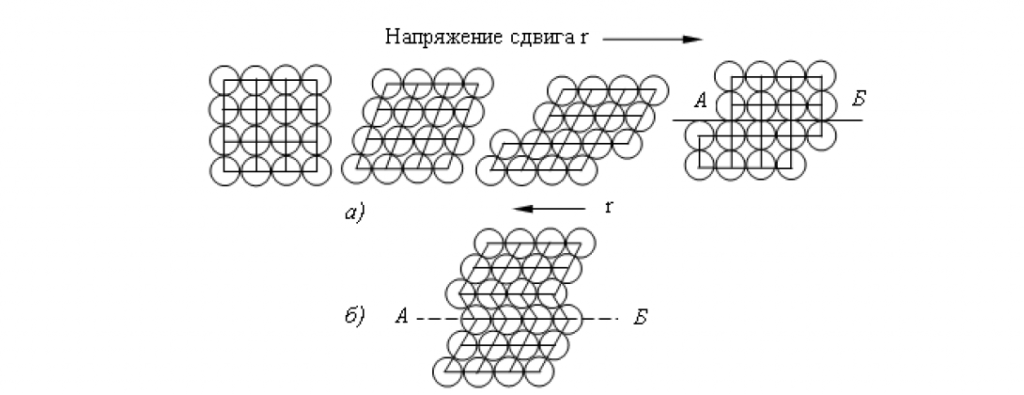
Таким образом, пластические деформации вызывают повышение плотности дислокаций, искажение кристаллической решетки и приводят к увеличению напряжения, при котором возможны дальнейшие деформации.
Второй способ — создание металлов и сплавов с бездефектной структурой, — является более прогрессивным. В настоящее время получают кристаллы небольших размеров (длиной 2-10 мм и толщиной 0,5-2,0 мкм), так называемые «усы», практически без дислокаций, с прочностью близкой к теоретической. Такие кристаллы нашли свое применение для армирования волокнистых композиционных материалов, в микроэлектронике и т. д.
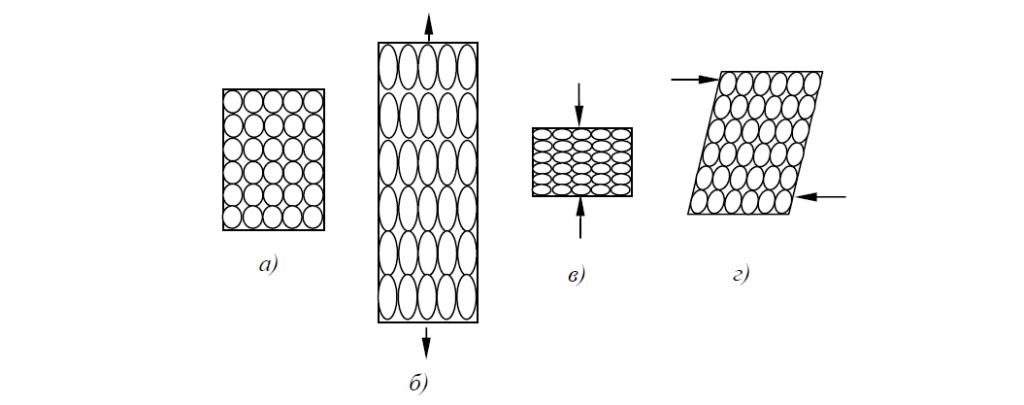
При деформировании округлые зерна заменяются вытянутыми в направлении деформации, образуется так называемая текстура (textura — ткань, связь, строение) — анизотропная поликристаллическая пли аморфная среда, состоящая из кристаллов или молекул с преимущественной ориентировкой. Текстуры могут: быть осевыми — с предпочтительной ориентировкой элементов текстуры относительно одного особого направления, плоскими — с ориентировкой относительно особой плоскости и полными — при наличии особой плоскости и особого в ней направления (рис. 2). Текстура создает анизотропию свойств.
Упрочненный металл обладает повышенным запасом внутренней энергии, т. е. находится в неравновесном состоянии. Для приведения металла в равновесное состояние его необходимо нагреть. При нагреве наклепанного металла в нем протекают следующие процессы:
- частичное восстановление структурного совершенства в результате уменьшения точечных дефектов за счет увеличения подвижности атомов (избыточные вакансии и межузельные атомы взаимодействуют между собой, а также поглощаются дислокациями при перераспределении последних при нагреве) и снижение внутренних напряжений (процесс возврата):
- уменьшение плотности дислокаций за счет аннигиляция противоположных по знаку дислокаций и образование субзерен (полигонов), свободных от линейных несовершенств за счет выстраивания дислокационных стенок (процесс полигонизации):
- зарождение и рост новых равноосных зерен вместо ориентированной волокнистой структуры деформированного металла (процесс рекристаллизации).
Процесс рекристаллизации начинается с образования зародышей новых зерен и заканчивается полным замещением деформированного зерна мелкими равноосными зернами (первичная рекристаллизация), в результате чего полностью снимается наклеп, созданный при пластическом деформировании (снижаются прочность и твердость металла и увеличивается его пластичность), металл приобретает равновесную структуру с минимальным количеством дефектов кристаллического строения. Плотность дислокаций после рекристаллизации снижается с 1010-1012 см-2 до 106-108 см-2.
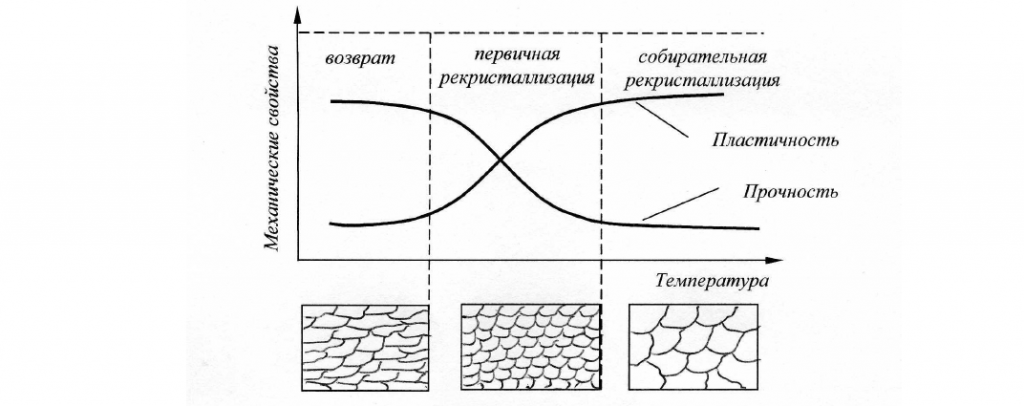
При дальнейшем повышении температуры происходит увеличение размеров наиболее крупных зерен за счет присоединения мелких. С повышением температуры число крупных зерен постепенно растет, пока все мелкие зерна не окажутся присоединенными к крупным — процесс вторичной (собирательной) рекристаллизации.
Температуру начала рекристаллизации, при которой протекает рекристаллизация, происходит разупрочнение холоднодеформированного металла и восстановление его пластичности называют температурным порогом рекристаллизации ТПР.
Эта температура не является постоянной физической величиной, как, например, температура плавления. Для данного металла (сплава) она зависит от длительности нагрева, степени предварительной деформации, величины зерна до деформации и т. д. Температурный порог рекристаллизации снижается с повышением степени деформации, увеличении длительности нагрева или уменьшении величины зерна до деформации.
Температура начала рекристаллизации ТПР для технически чистых металлов составляет примерно 0,4Тпл, для чистых металлов снижается до (0,1-0,2)ТПЛ, а для сплавов возрастает до (0,5-0,6)ТПЛ.